Bisucaberin: Bakteriální siderofor
Jiří Patočka
Bakterie jsou mikroorganismy, které potřebují železo, jako spousta jiných organismů (Messenger & Barclay, 1983). Železo je důležitým prvkem pro mnoho životních funkcí, včetně metabolických procesů a transportu kyslíku. Bakterie ho potřebují pro růst a provádění enzymatických reakcí v rámci svého metabolismu. Existují různé způsoby, jak bakterie získávají železo a jedním z nich je získávání železa z prostředí ve kterén žijí pomocí tzv. sideroforů (Prabhakar, 2020). Siderofory jsou látky, které mají schopnost vázat a transportovat ionty železa. Bakterie jsou známé tím, že produkují siderofory, aby získaly železo z okolního prostředí. Bakterie mohou vylučovat siderofory do prostředí ve kterém žijí a poté zpětně absorbovat ve forně komplexu siderofor-železo. Siderofory jsou klíčové pro ekonomiku železa v přírodě a hrají důležitou roli v boji organismů o získání tohoto důležitého prvku (Saha et al., 2013).
Každý živý organismus potřebuje železo, protože ionty tohoto v přírodě široce rozšířeného kovu mají velmi užitečné vlastnosti, hlavně redoxní. Jsou proto součástí mnoha metaloproteinů, které hrají klíčovou úlohu v metabolismu všech organismů. Získání železa z prostředí, v kterém organismy žijí, komplikuje jeho malá biologická dostupnost, která je daná především obecně špatnou rozpustností jeho kyslíkatých sloučenin. Proto si řada organismů, především bakterie (ale také některé houby a rostliny), vyvinuly schopnost produkovat a do svého okolí látky, které dokáží železo z okolního prostředí získat v podobě rozpustného železitého komplexu. Vzniklý železitý komplex je příslušnou bakterií vstřebán, uvnitř její buňky je rozložen a železo je následně použito pro konstrukci metaloproteinů. Těmto produkovaným nízkomolekulárním látkám se říká siderofory (řecky „nosiče železa“) a jejich tvorbu si organismus reguluje podle toho, jaký je aktuální stav jeho potřeb tohoto životně důležitého kovu. Většina aerobních a fakultativně (příležitostně) anaerobních mikroorganismů syntetizuje alespoň jeden siderofor.
Z mořských bakterií Alteromonas haloplanktis a Vibrio salmonicida byl izolován cyklický siderofor nazvaný bisucaberin a z bakterií Tenacibaculum mesophilum získaných z mořské houby byl získán jeho lineární analog, pojmenovaný bisucaberin B.
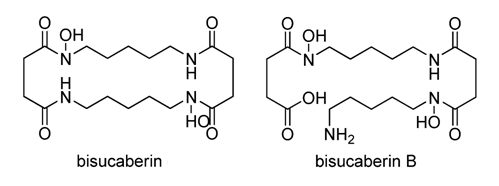
Bisucaberin B, který je otevřenou formou známého makrocyklického dimeru bisucaberinu byl již dříve popsán jako produkt bakteriální degradace desferrioxaminu B v bakterii Azospirillium irakanse.
V lidském organismu je volného železa minimum, je kompletně vázáno na proteiny a i jeho transport krví probíhá ve formě železitého komplexu s proteinem transferinem. Je to proto, že volné ionty železa mohou být toxické tvorbou reaktivních forem kyslíku, které pak poškozují tkáně. Proto je klíčovou schopností patogenní bakterie pro přežití v organismu její schopnost ukořistit pro sebe železo i v prostředí, kde je jeho biologická dostupnost malá, a hlavním nástrojem je právě tvorba sideroforů. Produkce bakteriosideroforů je tedy považována za jeden z nejdůležitějších faktorů patogenity, což činí jejich detekci velmi důležitou v diagnostice chorob bakteriálních a houbových infekcí.
Protože chemická struktura sideroforů se velmi liší, není přímá analytika pro jejich diagnostiku jednoduchá – vyžaduje standardy mnoha různých látek. Systém, který by byl schopen rychle a snadno detekovat produkci látky obecně schopné selektivně pevně vázat (chelatovat) železo, aniž by nutně znal strukturu konkrétního produkovaného sideroforu by byl pro diagnostiku velmi cenný.
Také pro člověka může být jak nedostatek, tak i nadbytek železa velmi nebezpečný. Takový nadbytek může vzniknout například v důsledku poměrně častého dědičného onemocnění hemochromatózy, kdy organismus kvůli poruše jednoho z regulačních genů ztratí kontrolu nad příjmem železa. Neřízený příjem železa pak vede k postupné intoxikaci, která následně poškodí játra a další orgány. Obvyklým způsobem léčby je flebotomie, známá jako „pouštění žilou“, při níž s krevním hemoglobinem odchází z těla i přebytečné železo (Bergeron et al., 2014). V řadě případů je ale nezbytné přistoupit i k farmakologické léčbě pomocí látek schopných železo na sebe pevně navázat (chelátorů železa). Takovým skutečně účinným a dodnes široce užívaným lékem na hemochromatózu je bakteriální siderofor desferrioxamin, produkovaný bakterií Streptomyces pilosus (Yu et al., 2008). Takovým lékem by mohly být i bisucaberiny (de Carvalho et al., 2011).
Literatura
Bergeron RJ, Wiegand J, McManis JS, Bharti N. Desferrithiocin: a search for clinically effective iron chelators. J Med Chem. 2014; 57(22): 9259-9291.
de Carvalho C, Marques M, Fernandes P. Recent achievements on siderophore production and application. Recent Patents Biotechnol. 2011; 5(3): 183-198.
Messenger AJ, Barclay R. Bacteria, iron and pathogenicity. Biochem Education, 1983; 11(2): 54-63.
Pešková S. Laboratorní diagnostika poruch metabolismu železa. Bakalářská práce, Univerzita Pardubice, 2022.
Prabhakar PK. Bacterial siderophores and their potential applications: a review. Curr Mol Pharmacol. 2020; 13(4): 295-305.
Saha R, Saha N, Donofrio RS, Bestervelt LL. Microbial siderophores: a mini review. J Basic Microbiology, 2013; 53(4): 303-317.
Yu Y, Wong J, Lovejoy DB, Kalinowski DS, Richardson DR. Chelators at the cancer coalface: desferrioxamine to Triapine and beyond. Clinical Cancer Research, 2006; 12(23): 6876-6883.